晶体生长理论——二维成核学说
出处:按学科分类—工业技术 中国轻工业出版社《制盐工业手册》第312页(1101字)
表面反应过程常常是晶体生长过程的控制阶段。解释晶体表面反应机理的一个重要学说是二维成核学说:“一个真实的晶体可以被想象为一个立方体,由许多小立方体堆砌而成,各小立方体可认为是微小的粒子,也可以是原子、分子、离子或分子团。每个小立方体有6个近邻,有6个面彼此接触。当一个新粒子添加到晶面上时,可能性最大的位置应该是能量最有利的位置,或者说是成键数最多的位置。”
由图2-5-17可见,最有利的添加位置是台阶的缺口(kink),如立方体(1)处,它有3个近邻,可以成键;第二个有利的位置是台阶的前缘,如立方体(2)处;最不利的位置是晶体表面上孤立的粒子位置,如立方体(3)处。完整晶面上既无台阶,更无缺口,形成新的粒子层只有从最不利的位置开始,当有一个粒子加到晶面上后,其他粒子就会迅速地加到台阶前缘或缺口处,而形成整个粒子层。最先加到晶面上的粒子可认为是一个二维生长的核,它是新晶层形成的开始。晶体的生长速率取决于晶面上二维生长的核的形成速率。二维成核的动力学方程式为:
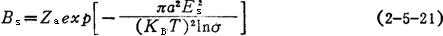
式中 BS——表面成核速率〔数目/(〔m2·s)〕
Za——表面处新粒子到达的速率〔数目/(cm2·s)〕
KB——Boltzman常数〔1.3806×10-16erg/(mol·k)〕
a2——单个粒子覆盖的面积(cm2)
Es——界面能(erg/cm2)
σ——相对过饱和度

图2-5-17 部分完成的晶体表面
根据上式所表达的二维成核定律,在低过饱和度范围内的晶体生长速率如图2-5-18中实线ab段所示。概括地说,只有过饱和度超过某一限度(如图中a点),生长始能进行;b点以上,生长速率与过饱和度近似地呈线性关系,因为在较高的过饱和度下,粒子碰撞晶面的频率已很高,表面生长的核经常存在。但大多数晶体的实际生长速率,却如图2-5-18中虚线所示,随所有过饱和度(包括低过饱和度)呈线性增长。
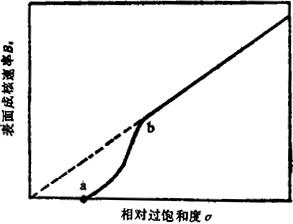
图2-5-18 二维(表面)成核速率与相对过饱和度的函数关系图